This store requires javascript to be enabled for some features to work correctly.
Cannabinoide wirken über das körpereigene Endocannabinoidsystem, eine komplexe Kommunikationsstelle zwischen Körper und Gehirn. Das Endocannabinoidsystem stellt das Gleichgewicht multipler Prozesse (Schmerzregulation, Schlafförderung, Nahrungszufuhr, Immunabwehr, Gedächtnis etc.) im menschlichen Körper ein.
Dieses Nervensystem besteht aus den sogenannten CB1 und CB2 Rezeptoren, über welche Cannabinoide wie ein Schlüssel andocken. Auch körpereigene Cannabinoide interagieren mit diesen Rezeptoren, wobei die Produktion dieser unter verschiedenen Einflüssen (z.B. Stress, Schlafmangel) reduziert sein kann.
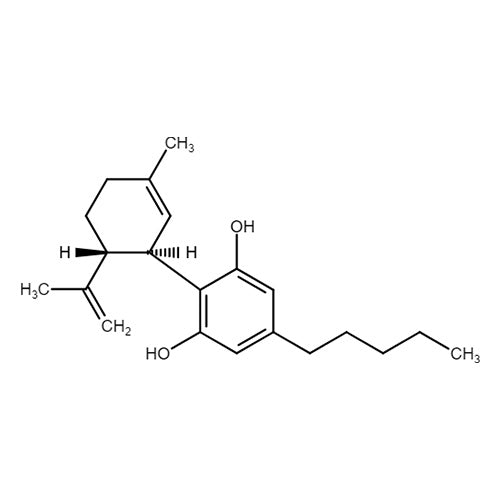
Cannabidiol (CBD) ist zusammen mit dem Tetrahydrocannabidiol (THC) einer der natürlichen Hauptbestandteile der Hanfpflanze. Im Gegensatz zu THC zeigt CBD keine berauschende (psychoaktive) Wirkung, vielmehr verringert es die psychoaktive Wirkung des THC. Studien der letzten Jahre legen CBD v.a. eine antiepileptische, antipsychotische und angstlösende Wirkung nahe. Ebenfalls beschrieben sind eine antientzündliche, schmerzlindernde, übelkeitsmindernde und muskelrelaxierende Wirkweise. Zu den Einsatzgebieten zählen so z.B. Epilepsie, Angsterkrankungen oder Schizophrenie.
Die Weltgesundheitsorganisation (WHO) beschreibt CBD als “allgemein gut verträglich” und mit einem “gutem Sicherheitsprofil” einhergehend. CBD ist legal und frei verkäuflich.
STUDIEN CBD
The National Academies of Sciences. Engineering, Medicine. The Health Effects of Cannabis and Cannabinoids: The Current State of Evidence and Recommendations for Research.Washington, DC: The National Academies Press; 2017.
WHO Expert Committee on Drug Dependence : CANNABIDIOL (CBD) Critical Review Report. Geneva: World Health Organization; 2018.
Whiting, Penny F et al. “Cannabinoids for Medical Use: A Systematic Review and Meta-analysis.” JAMA vol. 313,24 (2015): 2456-73.
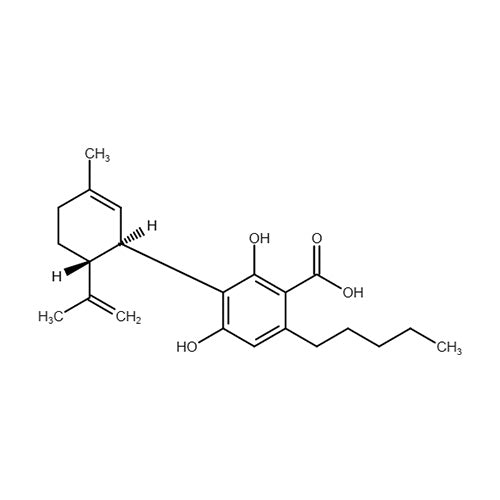
Die Cannabidiolsäure (CBDA) ist eine nicht-psychoaktive Vorstufe des CBDs. Die Studienlage über die Wirkweise von CBDA ist bislang rar, jedoch können erste studienbasierte Erfolge nachgewiesen werden. Eine Studie von 2013 zeigte so einen deutlichen Effekt gegen Übelkeit und Erbrechen, wobei sogar eine höhere Wirksamkeit als bei CBD erfasst wurde. Zudem nimmt man eine entzündungshemmende Wirkweise im menschlichen Organismus an. Aufgrund der ähnlichen Rezeptorbesetzung wie CBD zeigt auch CBDA eine schmerzlindernd und angstlösende Wirkung. 2022 erlangte CBDA neben CBGA im Rahmen einer Studie gegen Coronaviren Aufmerksamkeit, da die Viren vor dem Andocken an menschliche Zellen abgehalten werden konnten.
STUDIEN CANNABIDOLSÄURE (CBDA)
Bolognini, D et al. “Cannabidiolic acid prevents vomiting in Suncus murinus and nausea-induced behaviour in rats by enhancing 5-HT1A receptor activation.” British journal of pharmacology vol. 168,6 (2013): 1456-70.
Rock, Erin M et al. “Effect of cannabidiolic acid and ∆9-tetrahydrocannabinol on carrageenan-induced hyperalgesia and edema in a rodent model of inflammatory pain.” Psychopharmacology vol. 235,11 (2018): 3259-3271.
van Breemen, Richard B et al. “Cannabinoids Block Cellular Entry of SARS-CoV-2 and the Emerging Variants.” Journal of natural products vol. 85,1 (2022): 176-184.
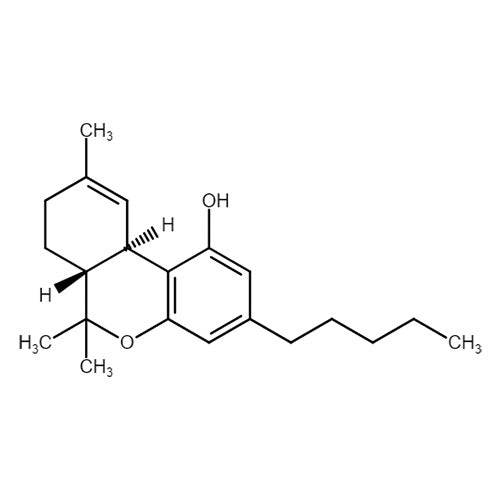
THC (Tetrahydrocannabinol) zählt zum Hauptbestandteil der Cannabispflanzen und gehört zu den wissenschaftlich am besten erforschten Cannabinoiden. Das THC stellt die psychoaktive Substanz der Pflanze dar, d.h. dass hierdurch ein Rauschgefühl entstehen kann. Medizinisch wirkt es durch die Besetzung der sog. CB1/2-Rezeptoren muskelentspannend (z.B. bei Muskelspastiken) und kann Übelkeit bzw. Brechreiz (z.B. im Rahmen von Chemotherapie) lindern. Neben einer schmerzlindernden Wirkung konnte in einigen Studien auch ein appetitsteigernder und schlaffördernder Effekt nachgewiesen werden. THC wird vermehrt bei Patienten mit nervenbedingten (neuropathischen) oder tumorbedingten Schmerzen eingesetzt, wobei auch andere Schmerzpatienten (z.B. mit Multipler Sklerose, Fibromyalgie, chronischen Wirbelsäulensyndromen) in das potentielle Patientenspektrum fallen. Andere Studien beschreiben u.a. einen lindernden Effekt bei Tic-Störungen, ADHS, chronischen Darmerkrankungen oder Migräne.
STUDIEN THC
Whiting, Penny F et al. “Cannabinoids for Medical Use: A Systematic Review and Meta-analysis.” JAMA vol. 313,24 (2015): 2456-73.
Plasse, T F. “Clinical use of dronabinol.” Journal of clinical oncology : official journal of the American Society of Clinical Oncology vol. 9,11 (1991): 2079-80.
Wang, Tongtong et al. “Adverse effects of medical cannabinoids: a systematic review.” CMAJ : Canadian Medical Association journal = journal de l'Association medicale canadienne vol. 178,13 (2008): 1669-78.
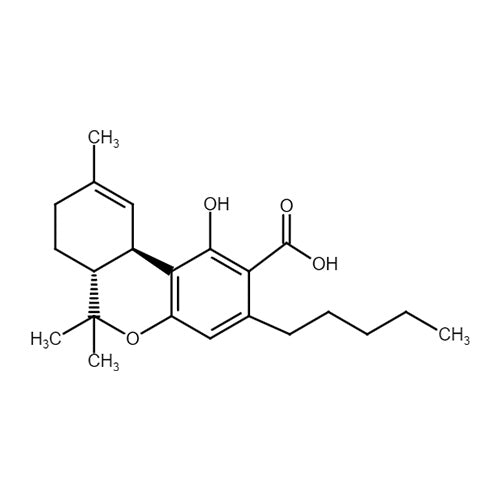
Tetrahydrocannabinolsäure (THCA) ist ein mit dem THC verwandtes Cannabinoid, was im Gegensatz zum THC aber nicht psychoaktiv wirkt. THCA ist eine saure Vorstufe des THCs und wird im Rahmen von Decarboxylierungsprozessen (Trocknung, Wärmezufuhr etc.) zu THC umgewandelt. Die Forschungen zu THCA stehen noch am Anfang, jedoch konnte in einigen Studien bereits eine muskelrelaxierende, entzündungshemmende und protektive Wirkungen an den Nerven nachgewiesen werden. Somit könnte THCA zukünftig somit v.a. bei neurodegenerativen und neuroinflammatorischen Erkrankungen eine Rolle spielen.
STUDIEN THCA
Nadal, Xavier et al. “Tetrahydrocannabinolic acid is a potent PPARγ agonist with neuroprotective activity.” British journal of pharmacology vol. 174,23 (2017): 4263-4276.
Moreno-Sanz, Guillermo. “Can You Pass the Acid Test? Critical Review and Novel Therapeutic Perspectives of Δ9-Tetrahydrocannabinolic Acid A.” Cannabis and cannabinoid research vol. 1,1 124-130. 1 Jun. 2016.
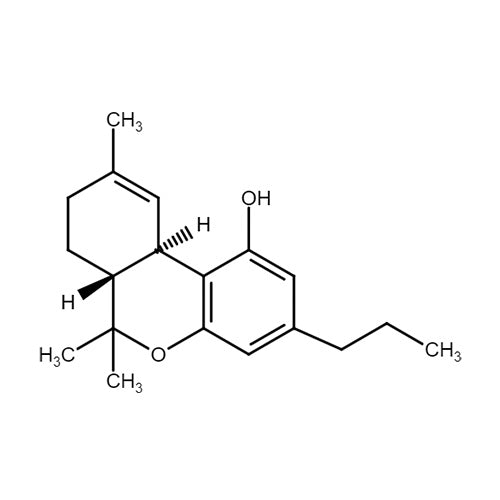
Tetrahydrocannabivarin (THCV) ist ein Cannabinoid, welches häufiger in Cannabis indica als in Cannabis sativa vorzufinden ist. Auch wenn die Molekularstruktur zu THC ähnlich ist, besitzt es seine eigene medizinische Wirkung. Im Gegensatz zu THC ist die Wirkung auf Rezeptoren dosisabhängig: Niedrige Dosierungen hemmen die Cannabinoid-Rezeptoren und somit die psychoaktive Wirkung, während hohe Dosierungen sich ähnlich zu THC verhalten können. Dieser „High-Zustand“ besitzt im Gegensatz zu THC eine kürzere Anhaltedauer und wird vom Patienten als luzide wahrgenommen. Derzeit wird ein vielversprechendes Potential bei der Therapie und Kontrolle von Typ-2-Diabetes diskutiert. In einer tierexperimentellen Studie aus dem Jahr 2013 konnte bei genetisch bedingten fettleibigen Mäusen die Glukoseintoleranz reduziert und die Insulinsensitivität verbessert werden. Bei neurodegenerativen Erkrankungen, wie Parkinson und Alzheimer, zeigte THCV in Tierversuchen bereits eine neuroprotektive und muskelkontrollierende Wirkung. Für abschließende Aussagen zur Wirksamkeit müssen jedoch klinische Studien folgen.
STUDIEN TETRAHYDROCANNABIVARIN (THCV)
Wargent, E T et al. “The cannabinoid Δ(9)-tetrahydrocannabivarin (THCV) ameliorates insulin sensitivity in two mouse models of obesity.” Nutrition & diabetes vol. 3,5 e68. 27 May 2013.
García, C et al. “Symptom-relieving and neuroprotective effects of the phytocannabinoid Δ⁹-THCV in animal models of Parkinson's disease.” British journal of pharmacology vol. 163,7 (2011): 1495-506.
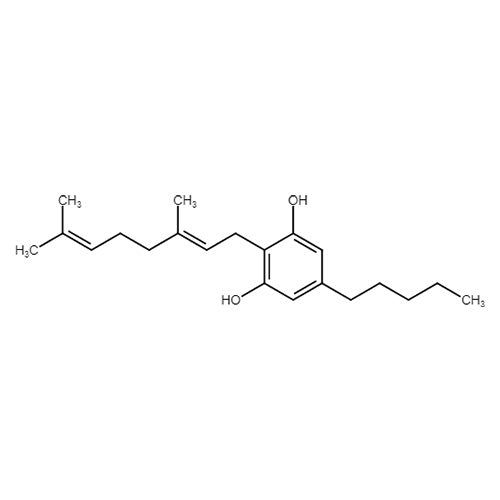
CBG (Cannabigerol) wirkt als nicht-psychotropes Cannabinoid und stellt eine Vorläufersubstanz von CBD, CBC, und THC dar. Über eine spezielle Rezeptorblockierung geht man von einer Verbesserung von Schmerz-, und Entzündungsprozessen aus. Antientzündliche Eigenschaften konnten bei entzündlichen Darmerkrankungen in Tierversuchen bereits erfolgreich nachgewiesen werden. CBG wird eine neuroprotektive Wirkung im Rahmen von neurodegenerativen Erkrankungen, wie Alzheimer, Multipler Sklerose und v.a. Chorea Huntington, zugeschrieben. Vergleicht man CBG mit anderen Cannabinoiden, zeigt es neben THCV den stärksten Effekt zur Erschlaffung der Blasenmuskulatur, was als Präventionsmethode bei Blasenerkrankungen eingesetzt werden kann. Auch eine Senkung des Augeninnendrucks konnte durch CBG nachgewiesen werden, was effektiv gegen den Grünen Star (Glaukom) ist. Im Rahmen von Krebserkrankungen wird eine krebsregulierende und appetitanregende Wirkung diskutiert. So konnte in einer tierexperimentellen Studie bereits eine Eindämmung der Vermehrung von Darmkrebszellen nachgewiesen werden.
STUDIEN CBG
Navarro, Gemma et al. “Cannabigerol Action at Cannabinoid CB1 and CB2 Receptors and at CB1-CB2 Heteroreceptor Complexes.” Frontiers in pharmacology vol. 9 632. 21 Jun. 2018.
Borrelli, Francesca et al. “Beneficial effect of the non-psychotropic plant cannabinoid cannabigerol on experimental inflammatory bowel disease.” Biochemical pharmacology vol. 85,9 (2013): 1306-16.
Valdeolivas, Sara et al. “Neuroprotective properties of cannabigerol in Huntington's disease: studies in R6/2 mice and 3-nitropropionate-lesioned mice.” Neurotherapeutics : the journal of the American Society for Experimental NeuroTherapeutics vol. 12,1 (2015): 185-99.
Pagano, Ester et al. “Effect of Non-psychotropic Plant-derived Cannabinoids on Bladder Contractility: Focus on Cannabigerol.” Natural product communications vol. 10,6 (2015): 1009-12.
Colasanti, B K. “A comparison of the ocular and central effects of delta 9-tetrahydrocannabinol and cannabigerol.” Journal of ocular pharmacology vol. 6,4 (1990): 259-69.
Brierley, Daniel I et al. “Cannabigerol is a novel, well-tolerated appetite stimulant in pre-satiated rats.” Psychopharmacology vol. 233,19-20 (2016): 3603-13.
Borrelli, Francesca et al. “Colon carcinogenesis is inhibited by the TRPM8 antagonist cannabigerol, a Cannabis-derived non-psychotropic cannabinoid.” Carcinogenesis vol. 35,12 (2014): 2787-97.
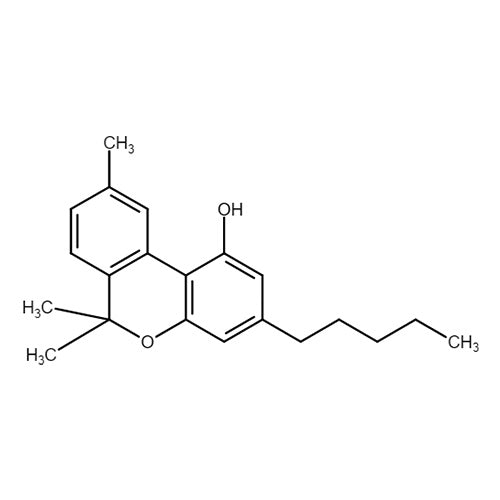
Cannabinol (CBN) ist ein leicht psychoaktives Cannabinoid und stellt ein Oxdationsprodukt von THC dar. Es befindet sich vor allem in getrocknetem, älterem oder erhitztem Cannabismaterial. Der Studienlage folgend, könnte CBN die stärkste beruhigende Wirkung unter den Cannabinoiden haben, was eine vielversprechende Behandlungsmöglichkeit von Angst- oder Stresszuständen oder Schlaflosigkeit darstellt. Neben eines schmerzlindernden Effekts ist auch ein antibakterielle Wirkung (z.B. gegen den Erreger MRSA) erfasst worden. Zusätzlich wird eine Wirksamkeit gegen Krampfanfälle, Glaukome oder Nervenerkrankungen (z.B. im Rahmen eine Ausbruchsverzögerung von der amyotrophen Lateralsklerose (ALS)) diskutiert. Tierexperimentell konnte zusätzlich eine appetitstimulierende Wirkung durch CBN erzielt werden.
STUDIEN CANNABINOL (CBN)
Appendino, Giovanni et al. “Antibacterial cannabinoids from Cannabis sativa: a structure-activity study.” Journal of natural products vol. 71,8 (2008): 1427-30.
Schier, Alexandre Rafael de Mello et al. “Cannabidiol, a Cannabis sativa constituent, as an anxiolytic drug.” Revista brasileira de psiquiatria (Sao Paulo, Brazil : 1999) vol. 34 Suppl 1 (2012): S104-10.
Weydt, Patrick et al. “Cannabinol delays symptom onset in SOD1 (G93A) transgenic mice without affecting survival.” Amyotrophic lateral sclerosis and other motor neuron disorders : official publication of the World Federation of Neurology, Research Group on Motor Neuron Diseases vol. 6,3 (2005): 182-4.
Elsohly, M A et al. “Cannabinoids in glaucoma: a primary screening procedure.” Journal of clinical pharmacology vol. 21,S1 (1981): 472S-478S.
Farrimond, Jonathan A et al. “Cannabinol and cannabidiol exert opposing effects on rat feeding patterns.” Psychopharmacology vol. 223,1 (2012): 117-29.
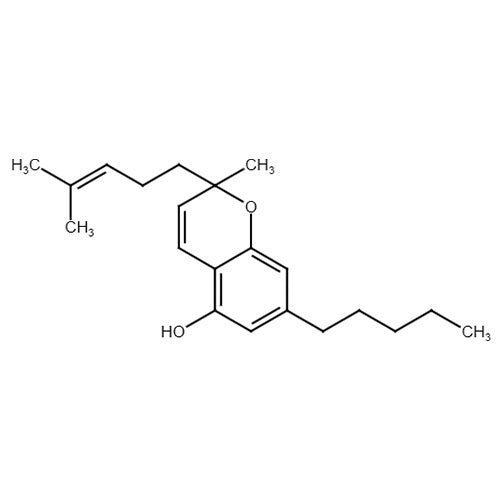
Das nicht-psychotrope Cannabichromen (CBC) entsteht aus dem Vorgängerstoff Cannabigerol (CBG). CBC konnte in Studien bereits eine schmerzstillende Wirkung durch das Angreifen an gewissen Zielproteinen nachweisen.
Die schmerzlindernde Potenz ist zwar nicht so hoch wie von Tetrahydrocannabinol (THC), konnte aber bei ausgewählten Krankheiten, z.B. mit einhergehendem Wirbelsäulenschmerz, eine signifikante Schmerzreduktion erzielen. Es verstärkt die Wirkung anderer Cannabinoide, so konnte bislang v.a. die antientzündliche Wirkung von THC stark erhöht werden. Andere Ergebnisse zeigten einen antimikrobiellen Effekt mit Wirksamkeit gegen therapieresistente Pilzen (z.B. schwarzen Schimmel), Kolibakterien und Staphylokokken eingesetzt werden. Auch eine antidepressive oder krebsbekämpfende Wirkung bei Brustkrebs werden diskutiert.
STUDIEN CANNABICHROMEN (CBC)
Maione, Sabatino et al. “Non-psychoactive cannabinoids modulate the descending pathway of antinociception in anaesthetized rats through several mechanisms of action.” British journal of pharmacology vol. 162,3 (2011): 584-96.
Russo, Ethan B. “Cannabinoids in the management of difficult to treat pain.” Therapeutics and clinical risk management vol. 4,1 (2008): 245-59.
DeLong, Gerald T et al. “Pharmacological evaluation of the natural constituent of Cannabis sativa, cannabichromene and its modulation by Δ(9)-tetrahydrocannabinol.” Drug and alcohol dependence vol. 112,1-2 (2010): 126-33.
DeLong, Gerald T et al. “Pharmacological evaluation of the natural constituent of Cannabis sativa, cannabichromene and its modulation by Δ(9)-tetrahydrocannabinol.” Drug and alcohol dependence vol. 112,1-2 (2010): 126-33.
Turner, C E, and M A Elsohly. “Biological activity of cannabichromene, its homologs and isomers.” Journal of clinical pharmacology vol. 21,S1 (1981): 283S-291S.
El-Alfy, Abir T et al. “Antidepressant-like effect of delta9-tetrahydrocannabinol and other cannabinoids isolated from Cannabis sativa L.” Pharmacology, biochemistry, and behavior vol. 95,4 (2010): 434-42.
Picardi, P et al. “Anandamide inhibits breast tumor-induced angiogenesis.” Translational medicine @ UniSa vol. 10 8-12. 8 Apr. 2014.
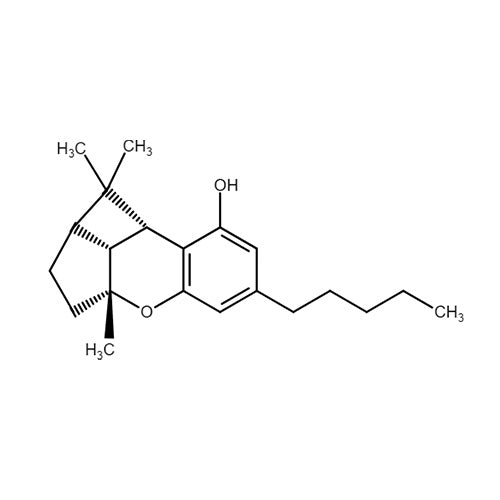
Das Phytocannabinnoid Cannabicyclol (CBL) stellt ein Abbauprodukt von Cannabichromen (CBC) dar, welches bei Hitzewirkung entsteht. Bis dato existieren nur sehr wenige Studien über CBL, von denen sich die meisten eher auf ihre chemische Zusammensetzung als auf ihre medizinische Wirkweise konzentrierten. Hiervon zeigten die meisten dieser Studien negative Ergebnisse, weshalb man davon ausgeht, dass die anderen Cannabinoide einen höheren medizinischen Stellenwert besitzen. Für ein tiefergehendes Verständnis müssen weitere Studien diesbezüglich folgen.
STUDIEN CANNABICYCLOL (CBL)
Morales, Paula et al. “Molecular Targets of the Phytocannabinoids: A Complex Picture.” Progress in the chemistry of organic natural products vol. 103 (2017): 103-131.
Vree, T B et al. “Identification of cannabicyclol with a pentyl or propyl side-chain by means of combined gas chromatography-mass spectrometry.” Journal of chromatography vol. 74,1 (1972): 124-7.
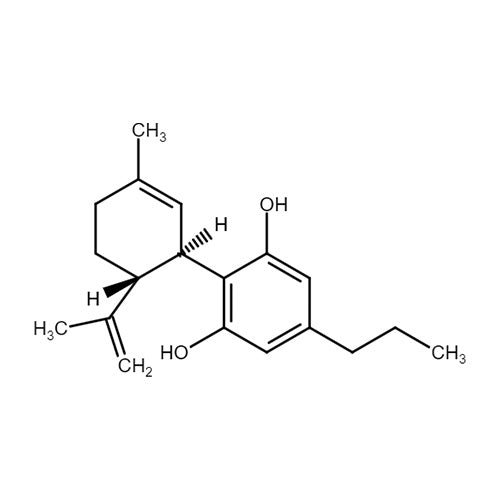
Cannabidivarin (CBDV) ist ein nicht-psychoaktives Cannabinoid. Die Studienlage zu CBDV befindet sich noch in ihren Anfängen, jedoch sind einige Studien medizinisch vielversprechend. So konnte man eine krampflösende Wirkung bei epileptischen Anfällen an Mäusen nachweisen, dessen Wirkung später in der Interaktion an den sog. TRP-Kanälen begründet wurde. Weitere Behandlungserfolge ließen sich bei Übelkeit, Autismus oder dem Rett-Syndrom, einer genetischen Erkrankung mit einer Entwicklungsstörung des Gehirns, nachweisen.
STUDIEN CANNABIDIVARIN (CBDV)
Iannotti, Fabio Arturo et al. “Nonpsychotropic plant cannabinoids, cannabidivarin (CBDV) and cannabidiol (CBD), activate and desensitize transient receptor potential vanilloid 1 (TRPV1) channels in vitro: potential for the treatment of neuronal hyperexcitability.” ACS chemical neuroscience vol. 5,11 (2014): 1131-41.
Hill, T D M et al. “Cannabidivarin-rich cannabis extracts are anticonvulsant in mouse and rat via a CB1 receptor-independent mechanism.” British journal of pharmacology vol. 170,3 (2013): 679-92.
Rock, Erin M et al. “Evaluation of the potential of the phytocannabinoids, cannabidivarin (CBDV) and Δ(9) -tetrahydrocannabivarin (THCV), to produce CB1 receptor inverse agonism symptoms of nausea in rats.” British journal of pharmacology vol. 170,3 (2013): 671-8.
Pretzsch, Charlotte M et al. “Effects of cannabidivarin (CBDV) on brain excitation and inhibition systems in adults with and without Autism Spectrum Disorder (ASD): a single dose trial during magnetic resonance spectroscopy.” Translational psychiatry vol. 9,1 313. 20 Nov. 2019.
Vigli, Daniele et al. “Chronic treatment with the phytocannabinoid Cannabidivarin (CBDV) rescues behavioural alterations and brain atrophy in a mouse model of Rett syndrome.” Neuropharmacology vol. 140 (2018): 121-129.

